Axit photphoric là hóa chất độc hại nhưng lại đóng vai trò đặc biệt quan trọng trong nhiều ngành công nghiệp hiện nay. Cùng tìm hiểu H3PO4 là gì, H3PO4 là chất điện li mạnh hay yếu? cũng như cách điều chế và ứng dụng cụ thể của axit này ngay bài viết sau đây!
Tóm tắt nội dung
H3PO4 là gì? Đặc điểm cấu tạo phân tử axit photphoric
H3PO4 là công thức hóa học của Axit photphoric, đây là loại axit có tham gia vào các phản ứng hóa học với nhiều chất, vì thế được ứng dụng nhiều trong các ngành công nghiệp hiện nay.
H3PO4 đọc là gì? H3PO4 được gọi là Axit photphoric, hay còn được gọi với những tên gọi khác như: trihiđroxiđioxiđophotpho, axit phosphoric, Axit orthophotphoric. Đây là một axit trung bình có công thcs hóa học là H3PO4 .
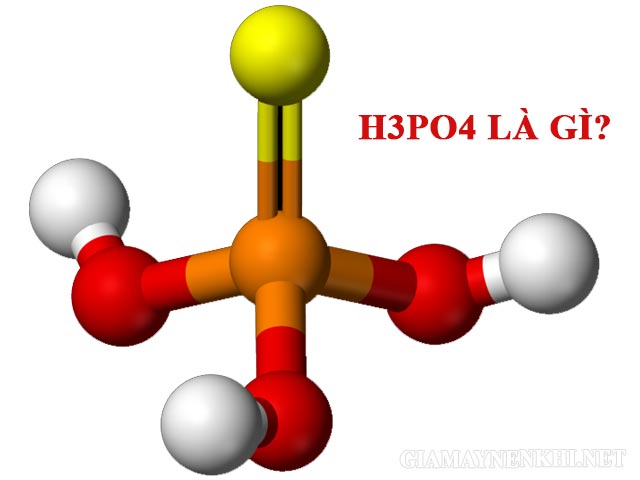
H3PO4 là axit mấy nấc? H3PO4 là một axit 3 nấc không có tính oxi hóa bởi chúng có cấu trúc không gian tứ diện, với độ mạnh trung bình.
Cấu tạo phân tử: Axit photphoric có 3 nấc phân li với cấu tạo phân tử gồm 3 phân tử hidro liên kết với gốc PO4.
Đặc điểm tính chất vật lý axit photphoric
Axit photphoric là chất tinh thể trong suốt, được tồn tại ở 2 dạng là chất rắn tinh thể không màu có thể tan vô hạn trong nước hoặc cồn với cấu trúc tứ diện đều và dạng thứ 2 là chất lỏng trong suốt không màu, có vị chua.
Thông thường, axit photphoric được dùng dưới dạng dung dịch đặc, sánh, không có màu, với nồng độ 85%. Đặc điểm tính chất vật lý khác của H3PO4 như sau:
- Axit photphoric háo nước, dễ chảy rữa và tan vô hạn trong nước theo bất kì tỉ lệ nào.
- Nhiệt độ nóng chảy: 42.5 độ C
- Nhiệt độ phân hủy: 213 độ C.
- Khối lượng riêng: 1.87 g/cm3

Tính chất hoá học của axit photphoric?
Phân li thuận nghịch
H3PO4 là axit mạnh hay yếu? Axit photphoric là một axit 3 nấc với độ mạnh trung bình. Trong dung dịch nước, H3PO4 phân li thuận nghịch theo 3 nấc cụ thể như sau:
Nấc 1: H3PO4 ↔ H+ + H2PO4– (Sự phân li chủ yếu)
Nấc 2: H2PO4– ↔ H+ + HPO42- (Sự phân li kém hơn)
Nấc 3: HPO42- ↔ H+ + PO43- (Sự phân li rất yếu)
Trong dung dịch Axit photphoric có các ion H+, H2PO4–, HPO42-, PO43- và những phân tử H3PO4 không phân li. Mặc dù không phải là một axit mạnh, nhưng khi ở nồng độ 85% chúng vẫn có thể gây ra những kích ứng nghiêm trọng cho da khi tiếp xúc.
Axit photphoric sở hữu đầy đủ tính chất của 1 axit
Axit photphoric có đầy đủ các tính chất hóa học của một axit như sau:
- Khiến cho quỳ tím bị chuyển sang màu đỏ
- Tác dụng với oxit bazơ giúp tạo ra sản phẩm muối và nước:
2H3PO4 + 3Na2O → 2Na3PO4 + 3H2O
- Khi tác dụng với bazơ tạo ra muối và nước, các sản phẩm muối khác nhau tùy theo tỷ lệ phản ứng như muối axit, muối trung hòa hoặc hỗn hợp các loại muối đó.
Ví dụ:
H3PO4 + KOH → KH2PO4 + H2O
2KOH + H3PO4 → K2HPO4 + 2H2O
3KOH + H3PO4 → K3PO4 + 3H2O

- Tác dụng với kim loại trước H2, sản phẩm được tạo ra là muối và giải phóng H2.
Ví dụ:
2H3PO4 + 3Mg → Mg3(PO4)2 + 3H2 ↑
- Tác dụng với muối tạo ra muối mới + axit mới.
Ví dụ:
H3PO4 + 3AgNO3 → 3HNO3 + Ag3PO4
- Phản ứng nhiệt phân: Ở nhiệt độ 200-250°C và 400-500°C, axit photphoric mang tính oxi hóa khử khi xảy ra phản ứng phân nhiệt:
2H3PO4 → H4P2O7 + H2O (nhiệt độ từ 200°C đến 250°C )
H4P2O7 → 2HPO3 + H2O (nhiệt độ từ 400°C đến 500°C )
H3PO4 là chất điện li mạnh hay yếu?
Giải đáp: H3PO4 là chất điện li yếu. Ta có phương trình điện li H3PO4 như sau:
H3PO4 ⇋ H+ + H2PO4– ⇒ k1 = 7, 6.10-3
H2PO4– ⇋ H+ + HPO42- ⇒ k2 = 6,2.10-8
HPO42- ⇋ H+ + PO43- ⇒ k3 = 4,4.10-13
⇒ nấc 1 −> nấc 2 −> nấc 3.
Cách điều chế axit photphoric
Điều chế H3PO4 trong phòng thí nghiệm
Điều chế axit photphoric trong phòng thí nghiệm bằng cách sử dụng HNO3 ra H3PO4 thực hiện như sau:
Dùng HNO3 đậm đặc để thực hiện oxy hóa photpho ở nhiệt độ cao:
P + 5HNO3 → H3PO4 + 5NO2 + H2O
Xem thêm: ▶ Cho Si vào bình chứa F2 tạo ra phản ứng & các ứng dụng gì
Điều chế axit photphoric ở trong công nghiệp
Trong công nghiệp, H3PO4 sản xuất chủ yếu bằng 2 phương pháp là quá trình nhiệt phương pháp khô và quá trình ẩm ướt như sau:
- Quá trình nhiệt
Phương pháp quá nhiệt P2O5 ra H3PO4 được thực hiện như sau:
Nguyên liệu sử dụng là Photpho và không khí, P được phun vào lò đốt cháy trong không khí ở nhiệt độ từ 1527°C – 2726°C để thu được diphotpho pentaoxit P2O5.

Sau đó, P2O5 được hòa tan trong dung dịch axit phosphoric loãng. Các phản ứng được diễn ra theo quy trình:
P → P2O5 → H3PO4
Cụ thể như sau:
4P + 5O2 → 2P2O5
P2O5 + 3H2O → 2H3PO4
Phương pháp nhiệt thường giúp tạo ra axit photphoric đậm đặc, tinh khiết hơn, bởi vì khi đốt ở trong lò điện, hầu hết tạp chất đã được loại bỏ. Phương pháp này có nhược điểm là tiêu tốn rất nhiều năng lượng.
Phương pháp ướt
Với phương pháp ướt sẽ sử dụng axit sunfuric để nhằm thực hiện phân huỷ khoáng calcium phosphate, chủ yếu được tìm thấy ở trong quặng apatit bên ngoài tự nhiên.
Axit photphoric được sản xuất từ fluorapatite Ca3(PO4)2 (đá phốt phát) bằng cách thêm axit sunfuric đậm đặc với nồng độ 93% vào trong một loạt các lò phản ứng được khuấy trộn.
Florua bị loại bỏ ở dưới dạng hợp chất không hòa tan là Sodium silicofluoride Na2SiF6. Chúng có thể được cô đặc để sản xuất H3PO4 thương mại, chứa khoảng 62% P2O5 với H3PO4 nồng độ 85%.
Tiếp tục loại bỏ nước tạo ra được axit superphosphoric với P2O5 nồng độ lớn hơn 70%, tương ứng với H3PO4 nồng độ 100%. Quá trình ẩm ướt tạo ra H3PO4 và canxi sulfate CaSO4 (thạch cao), cùng một số tạp chất không hòa tan khác.
CaSO4 dưới dạng sản phẩm phụ được loại bỏ dưới dạng phosphogypsum với phương trình phản ứng diễn ra như sau:
Ca5(PO4)3X + 5H2SO4 → 5CaSO4 + 3H3PO4 + HX
Ca3(PO4)2 + 3H2SO4 đặc → 3CaSO4 + 2H3PO4 (xúc tác nhiệt độ)
Axit thu được từ phương pháp trích ly mặc dù không tinh khiết nhưng vẫn sử dụng được mà không cần tinh chế thêm. Chúng thường được dùng để giúp sản xuất phân bón.
Ứng dụng của axit photphoric trong đời sống
Ứng dụng trong nông nghiệp
Khoảng 90% sản lượng axit photphoric trên thế giới dùng để thực hiện sản xuất phân bón. Chúng chủ yếu dùng để chuyển đổi thành ba loại muối phosphat sử dụng trong việc sản xuất phân bón superphosphat đơn và phân supephosphat kép. Ví dụ như: supe lân (TSP), diamonium hydrophosphate (DAP) và monoammonium dihydrogenphosphate (MAP),.. những loại phân này không chỉ được dùng để bón cho cây trồng, mà còn sử dụng để làm thành phẩm trong thức ăn gia súc.
Bên cạnh đó, H3PO4 cũng là chất được dùng trong việc sản xuất ra thuốc trừ sâu hiện nay.

Trong y tế
Axit photphoric chính là một thành phần cấu tạo trong xương và răng, chúng tham gia vào nhiều quá trình trao đổi chất. Axit photphoric có nồng độ dưới 35% thường dùng trong nha khoa và chỉnh hình răng, đóng vai trò là dung dịch khắc, giúp làm sạch và làm nhám cho bề mặt răng – nơi đặt thiết bị nha khoa hay các vật liệu trám răng. Bên cạnh đó, loại axit này cũng thường được sử dụng trong thuốc chống buồn nôn.
Trong mỹ phẩm
H3PO4 là một trong những thành phần có trong các sản phẩm làm sạch, thuốc nhuộm, nước hoa, cùng như một số sản phẩm trong làm móng, trang điểm, chăm sóc da,… chúng đóng vai trò là chất giúp thực hiện kiểm soát nồng độ pH.
Ứng dụng trong công nghiệp
H3PO4 ứng dụng trong công nghiệp với nhiều mục đích như:
Đây là chất phụ gia trong các loại đồ uống, mứt, thạch rau câu, pho mát hay chất tạo hương thơm cho thực phẩm bằng cách kết hợp với Hfcs (đã được xử lý enzyme) để nhằm tạo thêm vị ngọt.

Ứng dụng trong chất tẩm gỗ chống cháy, chất chống ăn mòn kim loại, là nguyên liệu trong việc sản xuất thuỷ tinh gạch men, xử lý nước, xi mạ, sản xuất các chất giặt tẩy.
Loại axit này giúp làm chậm sự phát triển của nấm mốc, vi khuẩn trong công thức đường, nên được ứng dụng để làm chất bảo quản.
Axit photphoric còn có tác dụng dùng để sản xuất các sản phẩm từ sữa. Muối của axit photphoric giúp thay đổi protein, độ pH, từ đó cải thiện chất lượng cho sản phẩm..
Xem thêm: Hóa trị là gì? Quy tắc xác định hóa trị các nguyên tố hóa học
Lưu ý quan trọng khi sử dụng axit photphoric
Axit photphoric có vai trò vô cùng quan trọng trong các ngành công nghiệp, nông nghiệp. Tuy nhiên, Axit photphoric là một loại axit rất độc, nếu sử dụng sai cách sẽ gây ra nhiều hậu quả nghiêm trọng như:
- Axit photphoric rất dễ bay hơi, khi tiếp xúc trực tiếp với H3PO4 sẽ gây ra tình trạng như: cay mắt, bỏng giác mạc, suy hô hấp, kích ứng, gây cháy nổ,… Nên trong quá trình sử dụng axit photphoric, người dùng cần trang bị đầy đủ đồ bảo hộ an toàn , cũng như kiến thức cần biết khi sử dụng loại axit này.

- H3PO4 là nguyên liệu có trong nước ngọt, là một trong những nguy cơ làm giảm mật độ xương. Cho nên, bạn cần hạn chế tối đa việc sử dụng các loại đồ uống ngọt đóng chai có chứa loại axit này.
- H3PO4 khi phản ứng ở nhiệt độ cao rất dễ gây ra tình trạng cháy nổ. Cho nên khi đã sử dụng xong bạn cần phải đóng bình cẩn thận, bảo quản chúng ở những nơi khô ráo, tránh ánh nắng trực tiếp.
- H3PO4 được dùng trong nhiều loại thực phẩm khác nhau, lượng Photpho trong các loại thức ăn này sẽ làm tăng nguy cơ mắc các bệnh như sỏi thận, tiết niệu,.. Lời khuyên là nên hạn chế thấp nhất việc sử dụng chúng để đảm bảo an toàn cho sức khỏe.
Qua bài viết này đã giúp bạn đọc hiểu được H3PO4 là gì, cũng như trả lời được cho câu hỏi H3PO4 là chất điện li mạnh hay yếu. Từ đó áp dụng tốt vào những bài tập liên quan.